人工知能(データ科学)×〇〇(1)「人工知能×ライフサイエンス」 ~個別化・層別化医療(ゲノム医療)とバイオインフォマティクス~
(2017年12月15日)
最近、人工知能(AI)に関するニュースをよく目にします。AIを支える情報処理技術は、機械学習、データ科学、統計科学、インフォマティクスなどいろいろな表現をすることができ、これらは今や分野を問わず科学研究になくてはならない道具になりつつあります。今回から2回にわたって、ライフサイエンス・医療の分野1)と物質・材料の分野のそれぞれについてAIがどのように使われようとしているかについて取り上げたいと思います。
「ゲノム医療」という言葉をご存じでしょうか?個人のゲノム(遺伝子のセット)を調べ、その結果をもとに、より効率的・効果的に病気の診断や治療などを行うことをいいます。現在の医療は、患者さんに対して、まずはこの薬を試してみましょう、効かなかったら違う薬を処方しましょう、というように治療が行われることがほとんどですね。例えば同じ「肺がん」でも複数の種類(サブタイプ)があって、さらに患者さんの遺伝子などのタイプによっても薬の効き方が異なることがあるからです。
ところが最近の研究では、患者さん個人のゲノムを調べて、この遺伝子タイプならこの薬が効く可能性が高いといったことがわかるようになってきました。また、「リキッドバイオプシー」といって、血液中の極微量のがんなどの病気を示唆する物質(がん細胞由来のDNAなど)を検出する技術の研究も進められています。
今後このような研究が進むと、将来的には普段の血液検査からがんなどの病気の診断や治療効果予測を行うことが可能になると期待されます。病気の早期の発見につながる他、無駄な薬が投与されることなく、患者さんにも、国の医療経済にもプラスになることが期待されています。このように個々の患者さんに適した医療を行うことを「個別化・層別化医療」あるいは「精密医療」と呼びます。
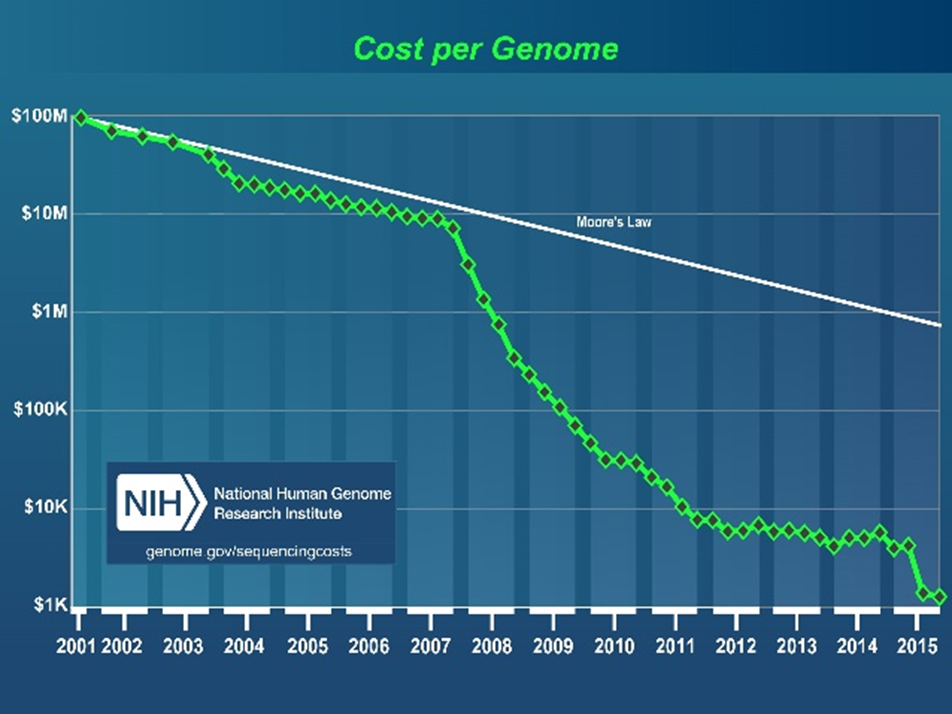
なぜ最近になってこのようなことが可能になったのか、背景には科学研究の飛躍的な進展があります。この20年で「DNAシーケンサー」と呼ばれるゲノムを調べる技術(最先端の半導体技術や物理化学的分析手法を統合したもの)と解析ソフトウェアが著しく発展し、ゲノムを特定する時間とコストが大幅に減少するとともに、正確さも年々上がっています。
米国を中心に1990年代に行われたヒトゲノム解読プロジェクトでは、2003年にヒトゲノムが解読されるまでに30億ドル(日本円で3,000億円超)もの研究費が投資されました。数年前には一人のヒトのゲノムを読むのに一週間程度、数十万円単位を要していたものが、最近では数時間、数万円からできるようになり、今後もさらに短時間、低コスト化していくと言われています。装置も昔は大型で場所を取るものでしたが、今では卓上型や手のひらサイズの装置が開発・販売されています。こうした状況から、今後、ゲノム医療がますます身近になっていくと考えられます。そして、たくさんのヒトのデータが集まることで、ゲノムと疾患の関係などいろんなことがわかるようになってくるでしょう。疾患と遺伝的要因や環境要因等の関連性の解明の成果を迅速に国民に還元するため、国の支援の下、様々な形でコホート研究(特定の地域や集団に属する人々を対象に、長期間にわたってその人々の健康状態と生活習慣や環境の状態など様々な要因との関係を調査する研究)が行われています(図2)。
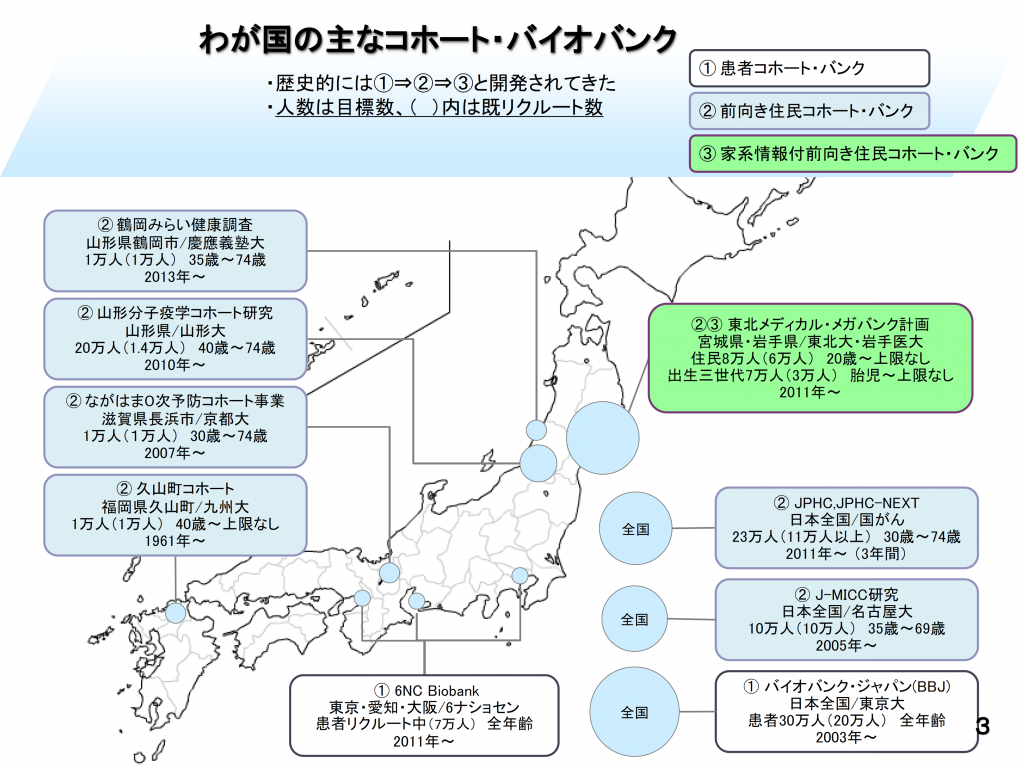
図22) わが国の主なコホート・バイオバンク
ヒトのゲノムは約30億の塩基対で構成され、個人差は約0.1%と言われています。
その多くは、ゲノム中に1000万箇所ある「一塩基多型(スニップ)」と呼ばれる塩基1つの違いです。この1カ所の違いだけが原因となる病気もありますし、複数の組み合わせで発症する病気もあると言われています。人間の目で全部を読み取るのはとうてい不可能なのでコンピュータを使いますが、このとき使うのが、「バイオインフォマティクス(生命情報科学);生物学のデータを情報科学の手法によって解析する学問および技術の総称」です。生物学では、ゲノム解析により大量のデータが生み出されるようになるとともに、この分野が急速に発展してきました。特にゲノムに対するインフォマティクスは進んでおり、ヒトのゲノム配列を特定したり、そのゲノム情報からどういう疾患リスクがあるか、あるいはどういう薬が効くかを調べたり、非常にたくさんの形で応用されています。一例として、東京大学医科学研究所では、IBM社が開発した人工知能「Watson」に、2,000万件以上の生命科学の論文、1,500万件以上の薬剤関連の情報を学習させ、がん患者の発病に関わる遺伝子や治療薬の候補を提示させる臨床研究を始めています。2016年、急性骨髄性白血病の60歳代の患者さんの遺伝子情報をWatsonに入力したところ、分析結果および治療方針を約10分で提示した、という例が報告されました。従来の人の調査や判断では、少なくとも2週間はかかる作業です。
いまはゲノム情報に基づく医療(臨床研究)が先行していますが、ゲノム情報だけではわからないこともたくさんあります。生体の遺伝的性質情報は、ゲノム情報からDNA⇒RNA⇒タンパク質という形で作られていきます。将来的には、ヒトの細胞内に存在するタンパク質やタンパク質群が構成する代謝のネットワーク情報(オミクス情報といいます)を見て、より個人に適した精密な医療を行う時代も来るかもしれません。ヒトの身体を構成する細胞・分子は種類も数も膨大で複雑なネットワーク(システム)を形成しています。今後AIを活用してこの複雑なネットワークが解明されることが期待されます。
【参考資料】
1) JST CRDS研究開発の俯瞰報告書「ライフサイエンス・臨床医学分野(2017年)3.2.1 ゲノム解析・オミクス解析、および3.5.6 予防・個別化医療」
https://www.jst.go.jp/crds/pdf/2016/FR/CRDS-FY2016-FR-06/CRDS-FY2016-FR-06_07.pdf
https://www.jst.go.jp/crds/pdf/2016/FR/CRDS-FY2016-FR-06/CRDS-FY2016-FR-06_10.pdf
2)内閣官房 健康・医療戦略室 第4回ゲノム医療実現推進協議会(平成27年7月15日)AMED提出資料https://www.kantei.go.jp/jp/singi/kenkouiryou/genome/dai4/siryou04.pdf
科学技術振興機構(JST)研究開発戦略センター(CRDS)
ライフサイエンス・臨床医学ユニット ユニットリーダー
島津 博基

島津 博基(しまづ ひろもと)
大阪大学大学院理学研究科を修了後、科学技術振興機構に入社。産学連携のファンディング事業(プロジェクト管理)を担当の後、情報分野、ナノテク・材料分野、環境・エネルギー分野の調査分析、戦略立案を経て、現職。弁理士試験合格。